
摘要:
细胞球包裹技术推动了用于研究组织生长的可控3D细胞培养模型的发展。在本案例研究中,研究人员采用液滴微流控方法,利用RayDrop包裹平台将哺乳动物细胞微流控包裹在海藻酸盐微珠中。该方法依赖于具有海藻酸盐核心和牺牲油壳的复乳(双重乳液),能够实现水凝胶的均质交联。被包裹的细胞保持存活,并在高弹性的海藻酸盐基质中增殖,最终形成多细胞球体。
波尔多大学、布鲁塞尔自由大学与Secoya Technologies合作论文
本研究由波尔多大学(Université de Bordeaux)、法国国家科学研究中心(CNRS)、布鲁塞尔自由大学(Université Libre de Bruxelles)与Secoya Technologies(一家致力于开发生物制药工艺实验室规模设备的衍生公司)合作完成。他们的RayDrop®微流控液滴发生器将Secoya的乳化技术集成到了一个易于使用的平台中,使得学术机构和研发实验室能够实现可重复的细胞球包裹和液滴生成。
哪些挑战限制了长期的3D细胞培养?
细胞球包裹是建立高重复性3D细胞培养模型的一项关键技术,这些模型包括用于再生医学的类器官,以及用于肿瘤学的多细胞球体(MCS)。与传统的2D培养相比,这些模型能更好地还原组织生理学特征,但其生产过程通常依赖于劳动密集型的实验方案,限制了其在高通量应用中的规模化。液滴微流控技术能够将细胞精确地包裹在水凝胶液滴中,在保持微环境可控的同时,支持细胞自组装形成细胞球。1–4
水凝胶支架(如海藻酸盐)可为长期的多细胞球体(MCS)培养提供重要的机械支撑和生化信号。然而,制备海藻酸盐微珠的传统方法通常会导致尺寸不均一,并且可能会损害细胞存活率(图1)。在微流控系统中使用复乳(双重乳液)的高阶策略虽然提高了微珠的均匀性,但如何在不影响细胞的前提下控制温和凝胶化仍然是一项挑战。5
尺寸和结构均一的单分散水凝胶微珠对于高质量的细胞球包裹至关重要,它们能确保营养物质的一致扩散以及最佳的细胞生长。将受控的微流控技术与具有生物相容性的水凝胶相结合,能够有效解决传统MCS生产方法的主要局限性(表1)。6,7
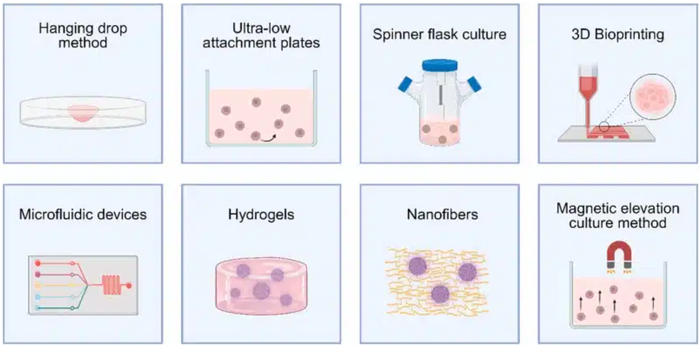
图1:当前制备3D细胞球策略的图解(Journal of Drug Delivery Science and Technology 2024, 100, 106033).
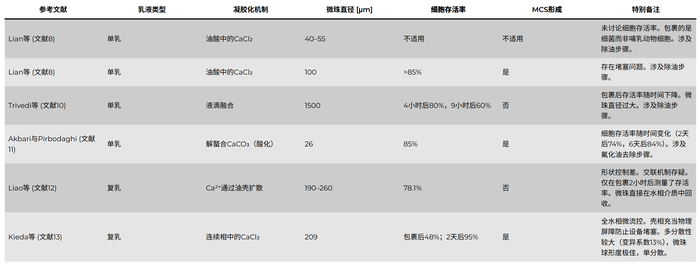
表1:当前在海藻酸盐微珠中进行细胞包裹的策略比较( Lab Chip, 2026,26, 711-724).
研究目的:用于细胞球包裹的牺牲油壳法
本研究旨在开发一种稳定、具有生物相容性,且适用于3D细胞培养系统中哺乳动物细胞的细胞球包裹方法。该研究优化了一种基于牺牲油壳的液滴微流控策略,通过控制钙离子跨越薄油壳的扩散,实现温和且均匀的水凝胶交联,从而生成均质的海藻酸盐微珠(图2)。这种方法能够实现高效的微流控包裹,同时保持细胞存活率并支持多细胞球体的形成。值得注意的是,该研究首次展示了使用非嵌入式毛细管几何结构来生产单分散且结构均质的海藻酸盐微珠,并证实其可兼容长期的细胞球培养。
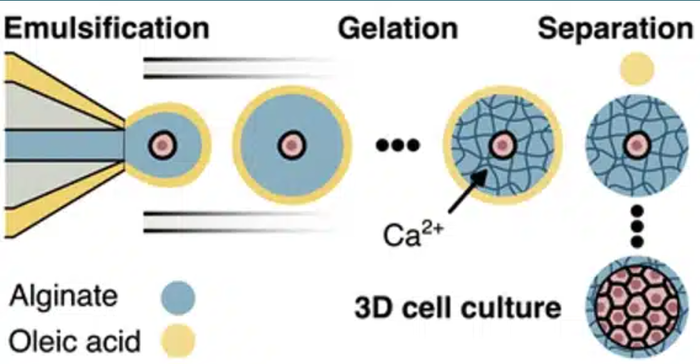
图2:适用于多细胞球体培养的海藻酸盐微珠的牺牲油壳生成法(Lab Chip, 2026,26, 711-724)
材料与方法:如何搭建用于细胞球包裹的微流控平台
实验使用哺乳动物HEK293T细胞进行3D细胞培养。细胞被重悬于无菌的海藻酸盐溶液中,以便后续将其包裹在水凝胶微珠内。
包裹过程使用RayDrop(由Secoya Technologies开发和制造)完成,这是一款基于毛细管、具有非嵌入式共焦聚焦几何结构的液滴微流控设备。该系统设有三个入口——分别用于引入核心相(细胞-海藻酸盐溶液)、壳相(油酸)和连续相(含表面活性剂的水溶液),以及一个用于收集微珠的出口(图3)。
使用Flow EZ压力控制器实现了对所有流体相的精确流量控制,保证了稳定的压力驱动注射和可重复的液滴形成。所有流体相均安装了在线过滤器,以去除颗粒物并防止设备堵塞。含细胞的核心相使用了带定量环的进样器进行进样,以防止细胞沉淀并确保均匀加载(图4)。
使用光学相机实时监测液滴的生成情况。微流控设备被配置为维持流体通过喷嘴进入提取毛细管时的同轴流动状态,从而确保复乳(双重乳液)液滴的正常形成。所有与细胞接触的管路和组件在使用前均经过了灭菌处理。

图3:使用RayDrop生产海藻酸盐微珠的五步法流程示意图,从复乳生成、Ca²⁺介导的凝胶化、油壳脱落到微珠回收 (Lab Chip, 2026,26, 711-724).
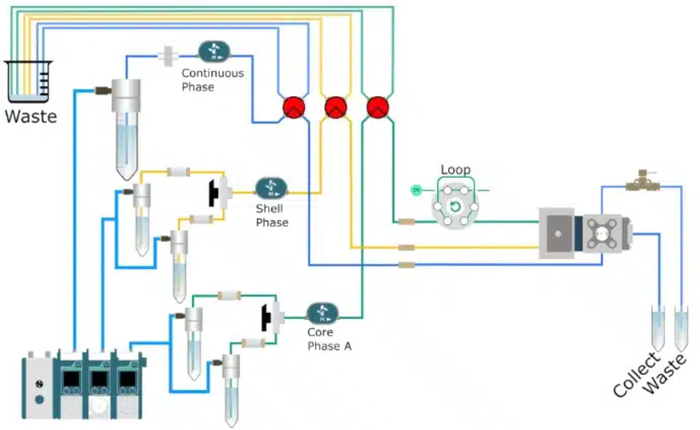
图4:带有进样环的RayDrop包裹平台。


Fluigent & Secoya 微滴制备平台Raydrop
概念验证:用于形成细胞球的哺乳动物细胞无螯合包裹
A- 海藻酸盐微珠中的细胞包裹
在液滴微流控技术生成的海藻酸盐微珠中,研究人员采用了无螯合物的CaCl₂(氯化钙)方法来包裹哺乳动物HEK293T细胞。该过程依赖于钙离子穿过包裹着海藻酸盐核心的牺牲油酸壳进行扩散(图5)。
利用RayDrop平台,通过同轴流动生成了复乳(双重乳液):海藻酸盐-细胞溶液形成核心相,油酸形成壳相,含表面活性剂的水相作为连续相。在受控的流速下(核心:25 μL/min;壳相:15 μL/min;连续相:300 μL/min),生成了直径在200至400 μm之间的单分散液滴。
钙离子从收集浴中穿过油酸壳扩散进去,诱导海藻酸盐发生缓慢且均匀的凝胶化。凝胶化完成后,油壳会自发脱落,通过温和离心即可回收微珠,从而获得结构均匀、呈球形且可直接用于培养的微珠。
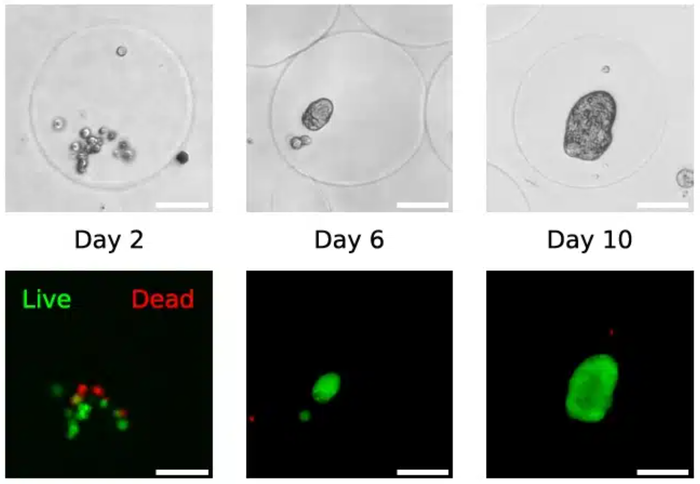
图5:细胞存活率与细胞球形成:HEK293T细胞在单分散海藻酸盐微珠中保持存活并形成细胞球。比例尺:100 μm (Lab Chip, 2026,26, 711-724).
B- 细胞球的形成与生长
被包裹的HEK293T细胞在具有弹性的海藻酸盐微珠内聚集并形成多细胞球体。细胞球的生长呈现指数趋势,这与预期的细胞分裂时间(约12-20小时)相符。较小的细胞球在很大程度上保持球形,而较大的细胞球由于受到水凝胶的机械约束,在圆度上会出现轻微的形变(图6)。
高弹性的海藻酸盐网络促进了在细胞球边界处形成超细胞F-肌动蛋白(F-actin)外壳,并限制了相邻细胞球之间的融合。这种方法确保了高细胞存活率、可重复的细胞球形成以及可控的生长动态,非常适合长期的3D培养研究。
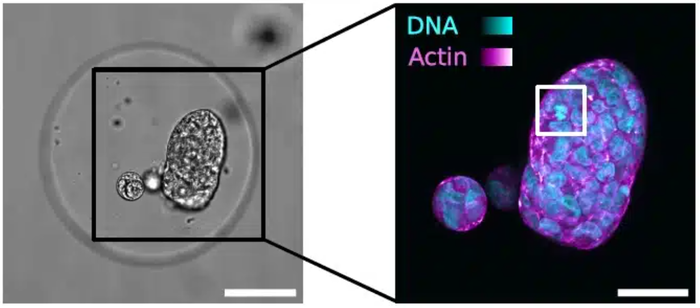
图6:HEK293T细胞球的生长动态:共聚焦赤道面视图展示了具有F-肌动蛋白外壳的多细胞球体。左图:肌动蛋白(灰度);右图:DNA(青色)与肌动蛋白(品红色)。比例尺:20 μm (Lab Chip, 2026,26, 711-724).
结论
本案例研究提出了一种实用且可重复的方法,通过结合RayDrop平台与Flow EZ压力控制器(用于精确流量调节),将哺乳动物细胞包裹在单分散、均质的海藻酸盐微珠中。Ca²⁺穿过油酸壳的缓慢扩散实现了均匀凝胶化,而油层的自发脱落让微珠的回收变得非常简单。该方法保持了很高的细胞存活率,支持长期的细胞球形成,并且可以在不需要事先掌握微流控专业知识的情况下,轻松地在标准生物实验室中实施,为研究组织形态发生学和3D细胞培养动态学提供了一项强大的工具。
相关文献/原文:
1. Rembotte, L.; Cappello, J.; Dewandre, A.; Mettler, M.; Septavaux, J.; Nassoy, P.; Scheid, B. Sacrificial Oil Shell Method for the Generation of Alginate Microbeads Adapted to Multicellular Spheroid Culture. Lab on a Chip 2026.
参考文献:
(1) Rembotte, L.; Cappello, J.; Dewandre, A.; Mettler, M.; Septavaux, J.; Nassoy, P.; Scheid, B. Sacrificial Oil Shell Method for the Generation of Alginate Microbeads Adapted to Multicellular Spheroid Culture. Lab on a Chip 2026.
(2) Lampart, F. L.; Iber, D.; Doumpas, N. Organoids in High-Throughput and High-Content Screenings. Front. Chem. Eng. 2023, 5. https://doi.org/10.3389/fceng.2023.1120348.
(3) Jensen, C.; Teng, Y. Is It Time to Start Transitioning From 2D to 3D Cell Culture? Front. Mol. Biosci. 2020, 7. https://doi.org/10.3389/fmolb.2020.00033.
(4) Fevre, R.; Mary, G.; Vertti-Quintero, N.; Durand, A.; Tomasi, R. F.-X.; Del Nery, E.; Baroud, C. N. Combinatorial Drug Screening on 3D Ewing Sarcoma Spheroids Using Droplet-Based Microfluidics. Iscience 2023, 26 (5)
(5) Chae, S.; Hong, J.; Hwangbo, H.; Kim, G. The Utility of Biomedical Scaffolds Laden with Spheroids in Various Tissue Engineering Applications. Theranostics 2021, 11 (14), 6818.
(6) Gadziński, P.; Froelich, A.; Jadach, B.; Wojtyłko, M.; Tatarek, A.; Białek, A.; Krysztofiak, J.; Gackowski, M.; Otto, F.; Osmałek, T. Ionotropic Gelation and Chemical Crosslinking as Methods for Fabrication of Modified-Release Gellan Gum-Based Drug Delivery Systems. Pharmaceutics 2022, 15 (1), 108. https://doi.org/10.3390/pharmaceutics15010108.
(7) Arora, S.; Singh, S.; Mittal, A.; Desai, N.; Khatri, D. K.; Gugulothu, D.; Lather, V.; Pandita, D.; Vora, L. K. Spheroids in Cancer Research: Recent Advances and Opportunities. Journal of Drug Delivery Science and Technology 2024, 100, 106033. https://doi.org/10.1016/j.jddst.2024.106033.
(8) Lian, M.; Collier, C. P.; Doktycz, M. J.; Retterer, S. T. Monodisperse Alginate Microgel Formation in a Three-Dimensional Microfluidic Droplet Generator. Biomicrofluidics 2012, 6 (4).
(9) Kim, C. Droplet-Based Microfluidics for Making Uniform-Sized Cellular Spheroids in Alginate Beads with the Regulation of Encapsulated Cell Number. BioChip J 2015, 9 (2), 105–113. https://doi.org/10.1007/s13206-015-9203-6.
(10) Trivedi, V.; Ereifej, E. S.; Doshi, A.; Sehgal, P.; VandeVord, P. J.; Basu, A. S. Microfluidic Encapsulation of Cells in Alginate Capsules for High Throughput Screening. In 2009 Annual International Conference of the IEEE Engineering in Medicine and Biology Society; IEEE, 2009; pp 7037–7040.
(11) Akbari, S.; Pirbodaghi, T. Microfluidic Encapsulation of Cells in Alginate Particles via an Improved Internal Gelation Approach. Microfluid Nanofluid 2014, 16 (4), 773–777. https://doi.org/10.1007/s10404-013-1264-z.
(12) Liao, Q.-Q.; Zhao, S.-K.; Cai, B.; He, R.-X.; Rao, L.; Wu, Y.; Guo, S.-S.; Liu, Q.-Y.; Liu, W.; Zhao, X.-Z. Biocompatible Fabrication of Cell-Laden Calcium Alginate Microbeads Using Microfluidic Double Flow-Focusing Device. Sensors and Actuators A: Physical 2018, 279, 313–320.
(13) Kieda, J.; Appak-Baskoy, S.; Jeyhani, M.; Navi, M.; Chan, K. W. Y.; Tsai, S. S. H. Microfluidically-Generated Encapsulated Spheroids (μ-GELS): An All-Aqueous Droplet Microfluidics Platform for Multicellular Spheroids Generation. ACS Biomater. Sci. Eng. 2023, 9 (2), 1043–1052. https://doi.org/10.1021/acsbiomaterials.2c00963.