
MIT Roger D. Kamm 团队在 Nature Protocols 发表了一套人源 BBB-on-chip 方法,并在实验中使用 Fluigent 的 Flow-EZ 压力式流体控制器,实现了对血管通透性的定量测量。这对基础研究与药物发现均是一条非常实用的路线。
作者构建了一个自组装的人源 BBB 微血管网络(microvascular networks, MVNs),用于系统评估各类分子跨屏障转运与通透性。模型由人源脑内皮细胞(可由干细胞分化或采用原代来源)与周细胞、星形胶质细胞共同建立,重点是复现人脑毛细血管的细胞组织、形态与转运功能,并给出可重复的通透性读数。整个实验流程包括器件制作(约1.5天)、培养(约7天)及成像/分子分析(最多5天),单个器件的一次通透性测量用时约30分钟。
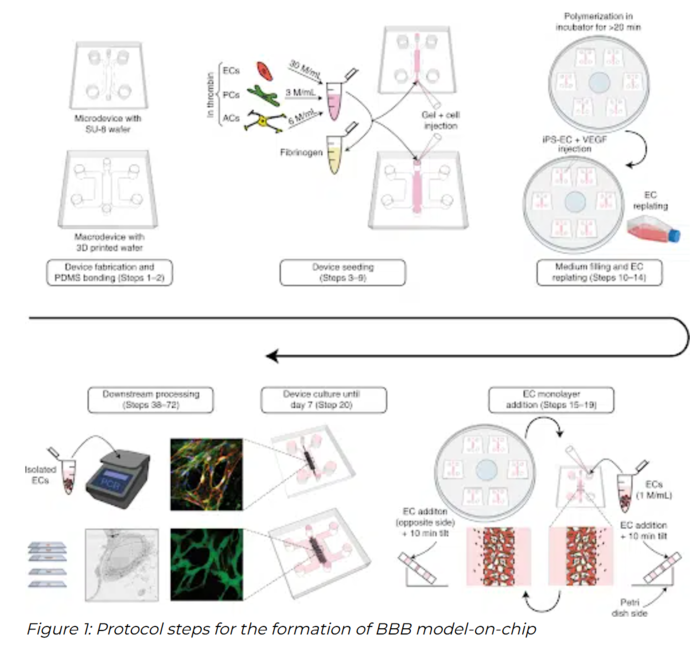
器件与细胞:采用软光刻制备带有中央凝胶区与旁侧灌流通道的 PDMS 微流控芯片;将纤维蛋白水凝胶与人脑周细胞、星形胶质细胞混匀后注入凝胶区并原位凝胶化;随后从旁侧通道播种人源脑微血管内皮细胞,使其在凝胶—通道界面自组织并腔化,形成可灌流的三维微血管网络。
结构尺度:培养约 7 天后,网络管径主要分布在约 10–40 μm,并呈现周细胞包覆与星形胶质足突接触等 BBB 相关形态特征。
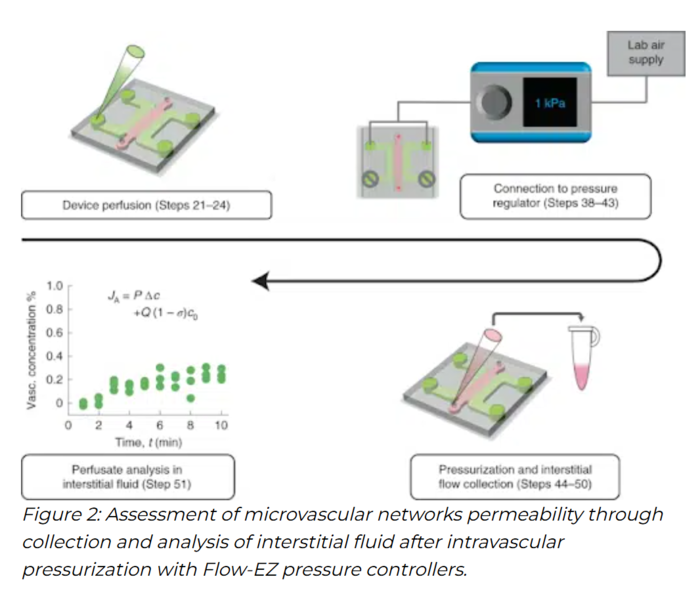
研究团队提供了两套互补读出方式:
1. 共聚焦成像法:灌注荧光示踪分子,直接成像并计算跨血管壁通量;
2. 加压采样法:用 Fluigent Flow EZ 在血管腔侧施加约 1 kPa 的稳定压力,产生生理相关的跨壁流;随后精准采集间质液,对其中的标记/非标记分子进行 ELISA 或质谱定量。
两种方法可联合使用,在生理跨壁流条件下得到有效通透性。
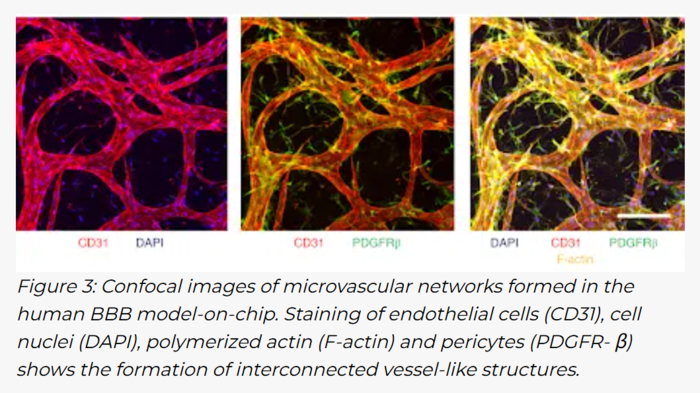
1. 与传统二维体系相比,该 BBB-on-chip 在细胞组织与形态、分子通透率等方面更接近体内水平,适合在学术与工业实验室广泛推广;
2. 在含有周细胞与星形胶质的培养条件下,iPS 来源的脑内皮细胞呈现更接近人原代脑内皮的基因/蛋白表达谱;
3. 通过对循环介质/间质液中的细胞因子进行多重检测(如 Luminex),还能关联炎症信号与转运体表达/通透性的变化。
在该文献中中,Flow-EZ 压力式控制器用于稳定灌流与定量加压采样,使研究者能在无脉冲波动的可控条件下完成分子通透性的测定,也为下游的蛋白/基因表达与分泌组学分析提供了可重复的流体环境。这类精确、灵活的压力控制,对维持三维微血管网络稳定、提升实验可重复性至关重要。
该平台可用于:
1. 纳米药物/生物大分子跨 BBB 的策略评估;
2. 病原体易感性与屏障破坏的研究(如 SARS-CoV-2 );
3. 在神经退行性疾病/神经炎症背景下,系统分析通透性、转运体与细胞因子网络的联动。
这项工作把将高生理相关性的人源 BBB 微血管模型与可量化、可复现的微流控通透性测量相结合:模型更接近体内,读出更标准化、可复现,也更贴近药物递送与安全性评价的实际需求。配合 Fluigent 的 Flow-EZ,研究者可以更快、更稳地获得高质量的通透性数据与机理线索。
想更系统地了解器官模拟 / OOC 方案、获得设备选型建议或演示?欢迎私信我们,或在评论区留言交流。也别忘了点赞、转发,关注我们的公众号,后续我们会持续分享更多 Organ-on-a-Chip / 微流控灌流 的最佳实践或案例。
相关文献:
1. Hajal C, Offeddu G S, Shin Y, et al. Engineered human blood–brain barrier microfluidic model for vascular permeability analyses[J]. Nature protocols, 2022, 17(1): 95-128.